1608
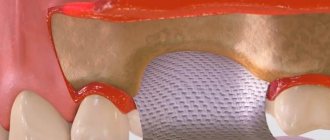
Барьерные мембраны – это современный хирургический тонколистовой материал, предназначенный для изоляции операционных ран, заполненных костным заменителем при направленной остеорегенерации.
Мембраны применяются для повышения эффективности костной регенерации, ускорения заживления ран, исключения резорбции костной ткани и послеоперационных осложнений.
Барьерные пленки используются в стоматологической хирургии при различных видах костной пластики, лоскутных операциях на пародонте, хирургической коррекции челюстно-зубных аномалий и пр.
Общее представление
Американская компания Osteogenics Biomedical производит различные по характеристикам барьерные мембраны из натуральных и искусственных материалов.
Резорбируемые материалы производятся из натурального сырья – сухожилий крупного рогатого скота и свиного коллагена.
Исходным материалом нерезорбируемых мембран является политетрафторэтилен. Материал из PTFE может иметь нетекстурированную и текстурированную поверхность, быть модифицирован (упрочнен) титаном.
Барьерные мембраны компании Osteogenics Biomedical
| Резорбируемые | Разм., мм | Нерезорбируемые | |||||
| Нетекстурированные | Разм., мм | Микротекстурированные | Разм., мм | Усиленные титаном | Разм., мм | ||
| Cytoplast RTM Collagen | 30х40, 20х30,15х20. | Cytoplast GBR-200 Singles | 12х24 | Cytoplast TXT-200 Singles | 12х24 | Cytoplast TI-250 ANTERIOR | 14х24, 12х24 |
| Cytoplast GBR-200 | 25х30 | Cytoplast TXT-200 | 25х30 | Cytoplast TI-250 BUCCAL | 17х25 | ||
| Cytoplast TI-250 POSTERIOR | 25х30, 20х25 | ||||||
| Cytoplast TI-250 XL | 30х40 | ||||||
Нерезорбируемая дентальная мембрана из политетрафторэтилена (PTFE) – является эксклюзивным продуктом, не производимым больше никем, кроме Osteogenics Biomedical.
Материал предназначен для направленной регенерации костной и десневой ткани при хирургических операциях в стоматологии.
В числе основных назначений Cytoplast GBR-200:
- обеспечение первичного покрытия раны;
- недопущение резорбции кости;
- стимулирование роста костной ткани из остеозаменителя;
- защита раны от болезнетворных микроорганизмов;
- ускорение заживления раны;
- упрощение работы хирургов.
Коррекция аномалий прикуса с помощью микроимплантов Vector Tas и особенности их использования.
Заходите сюда, если интересуют характеристики и назначение костного материала Bio Oss.
По этому адресу https://www.vash-dentist.ru/implantatsiya/metodiki/temperaturyi-posle-zubov.html узнайте, сколько держится температура после имплантации зубов при положительном исходе операции, и какие показатели указывают на необходимость обращения к врачу.
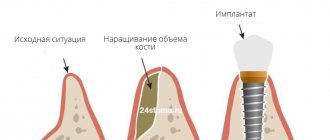
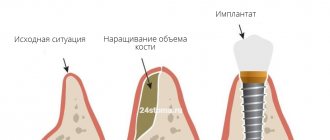
Успех реабилитации пациентов после дентальной имплантации определяется достаточным количеством костной ткани в участке имплантации.
Заполнение дефектов кости заменителями кости является процедурой выбора для поддержания кости, но врастание соединительной ткани из слизистой оболочки может нарушить процесс сращивания заменителя кости со стенками дефектов.
Использование мембраны для стоматологии в качестве барьера указывается в научной литературе как наиболее приемлемое решение данной проблемы.
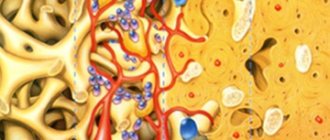
Направленная регенерация кости (НРК) — это метод, который основан на концепции отделения кости от мягких тканей, то есть предотвращение апикальной миграции эпителия десны и соединительной ткани внутри дефекта с мембраной в роли барьера. Использование мембраны способствует пролиферации клеток, способных к регенерации, и их дифференцировке в желаемый тип тканей.
Для направленной регенерации кости необходимо пять условий:
- Использование соответствующей мембраны;
- Достижение первичного заживления мягких тканей;
- Создание и поддержание участка, защищенного мембраной;
- Адаптация и стабилизация мембраны с окружающей костью;
- Достаточно длительный период заживления.
Согласно Hardwick и соавт., основная цель мембраны заключается в создании подходящих условий, при которых максимально реализуется естественный биологический потенциал функциональной регенерации.
Свойства и виды мембран для стоматологии
Создание и предварительная подготовка участка, где находится сгусток крови, предотвращение воспаления, которое может возникнуть в результате проникновения бактерий, изоляция пространства для регенерации от нежелательных тканей и обеспечение механической стабильности и компактности организованного коагулята — это лишь немногие из факторов успешной костной регенерации.
Следует упомянуть их роль в предотвращении проникновения эпителиальных клеток в костный материал, а также в усилении фиксации применяемого костного заменителя.
Обязательные свойства мембраны для стоматологии:
- Полная биологическая совместимость;
- Барьерная активность (профилактика пролиферации мягких тканей);
- Обеспечение соответствующей интеграции окружающих тканей;
- Способность сохранить участок для роста новой альвеолярной кости;
- Иммунологическая инертность;
- Простота применения.
Мембрана должна противостоять жевательной силе и сокращать натяжение тканей.
При этом критически важна способность мембраны интегрироваться с сохранением окружающих тканей и эффективно подавлять миграцию эпителия.
На основании клинических и гистологических исследований различных барьерных материалов, ни один из них не показал себя идеальным для каждой клинической ситуации. Каждый материал имеет определенные характеристики, преимущества и ограничения.
В зависимости от реакции на их биологическое окружение, мембраны могут быть сгруппированы как нерезорбируемые и резорбируемые.
Нерезорбируемые мембраны для стоматологии
сохраняют структуру и форму в тканях, и для их удаления необходимо провести еще одну операцию; это увеличивает травматичность, удлиняет заживление раны, повышает стоимость и продолжительность всего лечения.
Резорбируемые мембраны
не нужно удалять после размещения, что существенно повышает практичность и оптимизирует стоимость лечения, а также риск хирургических осложнений.
Из-за природы резорбируемых мембран невозможно точно определить продолжительность их разрушения. Процесс деградации начинается сразу после размещения.
Данные из литературы относительно желательной продолжительности персистенции мембраны in vivo показывают, что она варьирует от 4 недель до нескольких месяцев.
Из-за биологической деградации резорбируемые мембраны вызывают реакцию тканей, которая может отрицательно влиять на заживление раны и нарушать регенерацию.
Идеальная биорезорбируемая мембрана для направленной регенерации кости обладает следующими характеристиками:
- Биосовместимость;
- Отсутствие воспалительной реакции;
- Полная резорбция, деградация и элиминация;
- Высокая технологичность материала;
- Оптимальное время резорбции.
Такая стоматологическая мембрана должна быть простой в обращении, в том числе в очерчивании формы дефекта, поддержании требуемой формы и конфигурации. Она должна просто и надежно фиксироваться, быть устойчивой к бактериальной адгезии и колонизации.
Важнейшим требованием к мембранам является время резорбции, которое должно соответствовать срокам образования новой костной ткани.
Для производства резорбируемых мембран используют два материала: синтетический алифатический полиэфир и коллаген из различных животных источников, в том числе из бычьего сухожилия, бычьей дермы, телячьей кожи или свиной дермы.
Коллагеновые мембраны для стоматологии
Коллаген является нерастворимым волокнистым белком, который выступает важным природным компонентом соединительной ткани.
Способность коллагена стимулировать адгезию, хемотаксис и физиологическую деградацию клеток-предшественников наряду с возможностью деградации делает его идеальным материалом для создания мембран для стоматологии.
Существует, по меньшей мере, 16 типов коллагена, обнаруженных в интерстициальных тканях, матриксе кости, хряще, эпителиальных, кровеносных сосудах, стекловидном теле глаза. Коллаген I, II и III типов составляет 80–90% коллагена организма.
Доступные на рынке коллагеновые продукты состоят в основном из коллагена I и III типа.
Коллаген отличается слабой иммуногенностью, активирует гемостаз и может увеличивать толщину ткани. Во время заживления раны происходит клинически значимое взаимодействие коллагена с различными типами клеток.
Коллаген производится из кожи животных или субпродуктов. Сначала материал выделяют и очищают ферментами и химическими веществами, затем обрабатывают различными путями.
Наиболее распространенная химическая модификация коллагена формирует поперечные соединения, как правило, при воздействии альдегида, который уменьшает поглощение воды, влияет на способность к расплавлению, скорость деградации и стабильность.
Этот модифицированный материал называется поперечно сшитым коллагеном.
Коллагеновые мембраны разлагаются макрофагами и полиморфно-ядерными нейтрофилами, и скорость поглощения различается в зависимости от источника и модификаций коллагена.
Резорбция коллагеновой мембраны начинается с воздействия фермента коллагеназы (матрикс-металлопротеиназа), которая делит молекулу коллагена в определенном положении. Образующиеся части денатурируются и превращаются в желатин, который затем разлагается на аминокислоты желатиназой и другой протеиназой.
Во время ферментативного расщепления он включается в лоскут для поддержки прикрепления новой соединительной ткани. Это может привести к увеличению толщины лоскута, который защищает и обеспечивает дальнейшее образование костной ткани.
Сшивание коллагена: за и против
Стабильность структуры, повышенная за счет сшивания, замедляет процесс деградации.
Суть этого процесса заключается в создании различных взаимных связей между конкретными аминокислотами, а также между аминокислотами и карбоксилатными группами, под воздействием химических и физических агентов.
Сшивание коллагена достигается ультрафиолетовым и гамма-излучением, гексаметиленглутаральдегидом, дифенилфосфорилазой и рибозой.
Такая обработка снижает in vivo скорость резорбции коллагенового материала и повышает механические характеристики. В западном научном мире до сих пор существуют споры по поводу того, применять мембраны для НРК из сшитого или несшитого коллагена.
Многие исследования доказали, что при перекрестном сшивании биодеградация мембраны коллагена удлиняется, и что это показывает положительное, хотя и ограниченное влияние на НРК в различных типах экспериментальных моделей дефектов. Другие исследования свидетельствуют, что их использование связано с начальной реакцией инородного тела, ухудшает интеграцию тканей и трансмембранную васкуляризацию.
Несмотря на все расхождения, было показано, что васкуляризация мембраны улучшается через 2 недели после ее подслизистой имплантации на крысиной модели. Вероятно, это связано с тем, что первоначальная гиперемия в соседней ткани направляет ангиогенез в направлении экспериментальной мембраны.
В 2006 году Schwarz и соавт. исследовали модель ангиогенеза в природных и поперечно сшитых коллагеновых мембранах, потому что предыдущие тесты показали, что васкуляризация в сшитых мембранах протекает слабее.
Исследователями был сделан вывод, что скорость ангиогенеза при использовании разных типов мембран не имеет статистически значимых отличий.
В исследованиях, проведенных сотрудниками Военно-медицинской академии Белграда, дефекты, покрытые сшитыми коллагеновыми мембранами, продемонстрировали лучший уровень васкуляризации по сравнению с несшитыми мембранами и пустыми дефектами.
В 2012 году Thoma и соавт. изучали различия в сшитом коллагене, применяя материал различной степени сшивания в мягких тканях мышей.
Проведенные гистопатологические и гистоморфометрические анализы через 3 и 6 месяцев после вмешательства показали, что степень сшивания материала обратно пропорциональна интеграции тканей, степени биодеградации коллагена и скорости образования сосудов.
Коллаген с наиболее низкой степенью сшивания демонстрирует лучшую интеграцию окружающей ткани, стабильность и ангиогенез.
Несмотря на несколько отрицательных характеристик, многие авторы предположили, что использование сшитых коллагеновых мембран имеет много преимуществ в направленной регенерации костной ткани.
Эффективность коллагеновых мембран
Некоторые пародонтальные микроорганизмы продуцируют коллагеназу — фермент, который может привести к преждевременной деградации мембраны. Это, в частности, Porphyromonas gingivalis и Bacteroides melaninogenicus.
Бактериальная колонизация может привести к ранней деградации коллагеновых мембран, поставив под угрозу процедуру. Как сшитые, так и несшитые мембраны для стоматологии подвергаются лизису в равной степени под воздействием бактериальных протеаз, хотя сшитые мембраны несколько более устойчивы к протеолизу.
Терапевтические концентрации антибактериальных агентов, в том числе хлоргексидина, миноциклина и доксициклина, частично подавляют ферментативную деградацию мембран.
Коллагеновые мембраны различаются по микроархитектуре (пространство между молекулами коллагена, волокнами, пучками и слоями) и поперечной сшиванию.
Микроархитектура и сшивание определяют характеристики мембраны, такие как сила натяжения, простота использования, гибкость, интеграция тканей и биодеградация.
Мембраны с более высокой степенью сшивания остаются целостными в течение более длительного периода времени. Исследования показали, что преждевременная резорбция мембраны или ее удаление могут привести к неполному заживлению кости, поэтому рекомендуется, чтобы стоматологические мембраны, применяемые в НРК, имели период деградации от 3 до 9 месяцев для полноценного формирования кости.
Биодеградация коллагеновых мембран
Rothamel и соавт. изучали биодеградацию с течением времени, реакцию ткани, тканевую интеграцию и васкуляризацию доступных на европейском рынке коллагеновых мембран, а также экспериментальных продуктов, используя крысиные модели.
Гистологические и гистометрические исследования проводились через 2, 4, 8, 16 и 24 недели после размещения мембраны. Был сделан вывод, что сшитые коллагены I и III типа коровьего и свиного происхождения удлиняют процесс биодеградации, но снижают тканевую интеграцию и васкуляризацию.
Кроме того, при использовании указанных продуктов в экспериментах возникает реакция инородного тела, которая характерна для сшитых мембран.
Это исследование подчеркиваетупомянутые различия между сшитыми и несшитыми мембранами, доказывая, что несшитые мембраны имеют лучшую васкуляризацию и тканевую интеграцию. Скорость поглощения прямо коррелирует со степенью сшивания — чем выше уровень связей, тем больше скорость резорбции.
В 2006 и 2008 годах Tal и соавт. клинически и гистологически изучали продолжительность барьерной функции мембран и биоинтеграцию в местах, которые были обработаны сшитыми и несшитыми коллагеновыми мембранами.
Особое внимание было уделено спонтанным перфорациям слизистой через барьерные мембраны. Было показано, что сшитые мембраны были более устойчивы к деградации тканей и что они сохраняли целостность в течение более длительного периода.
Недостатки коллагеновых мембран для стоматологии
По сравнению с нерезорбируемыми мембранами, коллагеновые мембраны не обладают способностью поддерживать объем. Применение костного трансплантата для сохранения пространства имеет тенденцию улучшать исход направленной регенерации кости.
Увеличение альвеолярного отростка можно ожидать в том случае, если пространство под коллагеновой мембраной создается и сохраняется строго в соответствующий период, пока формируется новая кость.
Поэтому целесообразно использовать материалы, которые обеспечат поддержку, чтобы предотвратить разрушение барьера из-за давления, создаваемого жевательной силой.
Сегодня мембраны для стоматологии обычно используются с различными костными трансплантатами и наполнителями. Когда биорезорбируемые мембраны идут в такой комбинации, результаты НРК оказываются намного более благоприятными, и сопоставимыми с нерезорбируемыми мембранами.
Это особенно справедливо при лечении локализованных горизонтальных дефектов.
При этом сами по себе остеопластические материалы менее эффективны, чем комбинация вспомогательного материала и барьера. Комбинация мембран с костным материалом помогает достигать хороших результатов при лечении вертикальных дефектов альвеолярного отростка, поскольку одним из основных недостатков коллагеновой мембраны является неспособность достичь вертикальной высоты кости.
Для решения этой проблемы была использована упомянутая комбинация. Мембраны в этих случаях нуждаются в дополнительной стабилизации с помощью мини-винтов.
Влияние толщины мембраны на регенерацию кости
До сих пор не было опубликовано достаточно исследований о влиянии толщины резорбируемой мембраны на регенерацию кости.
Попытка применения более толстой мембраны была впервые опубликована в 2005 году Busenlechner и соавт. Цель их исследования состояла в том, чтобы поставить под сомнение возможности медленно рассасывающегося прототипа трехслойной мембраны при регенерации костной ткани.
В качестве модели использовалась процедура увеличения альвеолярного отростка после экстракции первого и второго коренных зубов в нижней челюсти обезьяны. Экспериментальных животных умерщвляли через 9 месяцев.
Результаты исследования поддерживают использование медленно рассасывающейся трехслойной мембраны, потому что наилучшая достигнутая регенерация кости была достигнута с помощью этой мембраны и костного трансплантата.
Мембрана была изготовлена путем добавления полилактидного слоя между слоями коллагена, чтобы увеличить время биодеградации, а также барьерную функцию.
Фрагменты полилактидов были обнаружены при гистологических исследованиях даже через 9 месяцев после выполнения хирургического вмешательства.
Усовершенствование конструкции трехслойной мембраны может быть важным шагом в улучшении стабильности мембраны с определенной скоростью воздействия.
Тот же прототип трехслойной мембраны был изучен von Arx и соавт. В ходе их исследования рассматривался прототип трехслойной мембраны в сочетании с различными материалами.
Отличия анализировали гистопатологически и гистоморфометрически через четыре с половиной месяца. Прототип трехслойной мембраны в сочетании с аутотрансплантатом продемонстрировал лучшую регенерацию кости.
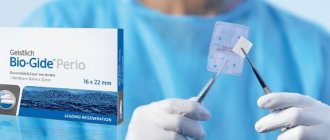
В 2009 году Козловский и соавт. провели гистологическое сравнение биодеградации мембраны Bio-Gide® (несшитой коллагеновой мембраны), которую использовали в один либо в два слоя с механическими дефектами, созданными на челюстях крысы.
Нанесение второго слоя мембраны Bio-Gide® (двухслойная техника) привело к значительному увеличению остаточного количества коллагена.
Также в ткани осталось больше барьерного материала, что указывает на более длительную барьерную функцию мембран, а также на то, что однослойная мембрана не может достичь аналогичной барьерной функции в течение длительного периода времени.
Таким образом, двухслойная мембрана для стоматологии существенно улучшает регенерацию костной ткани и не влияет на оссификацию. Следует отметить, что второй слой способствует уменьшению микроперемещений и увеличивает стабильность материала.
Трансмембранная васкуляризация проявлялась гистологически уже через 4 недели после имплантации и становилась четко выраженной через все слои мембраны спустя 9 недель после имплантации.
Несмотря на разницу в толщине двухмембранных препаратов, одинаковая степень деградации 80% для обеих мембран была достигнута уже через 9 недель.
Поскольку трансмембранное образование кровеносных сосудов необходимо для резорбции коллагена, представляется, что васкуляризация двухслойной мембраны не была нарушена из-за ее увеличенной толщины.
Утверждалось, что увеличение плотности поперечных связей между молекулами коллагена отрицательно влияет на биосовместимость, интеграцию мембраны, васкуляризацию, а также ингибирует прикрепление и пролиферацию фибробластов и остеобластов.
Использование второго слоя резорбируемой сшитой мембраны позволяет избежать этих недостатков, увеличивая долговечность стоматологической мембраны.
Эффективность двухслойных мембран при применении костных трансплантатов с точки зрения резорбции кости была проанализирована в исследованиях на кроликах.
Костные блоки теменных костей были взяты с одной стороны и помещены на другую, где покрыты мембранами. Гистологический и гистоморфометрический анализ проводили через 2, 4 и 6 месяцев после хирургического вмешательства.
Результаты исследования показывают, что применение двойных мембран значительно снижает резорбцию костной ткани трансплантата по сравнению с однослойным.
Другое исследование, проведенное сотрудниками ВМА Белграда, рассматривало воздействие коллагеновых мембран различной толщины. Результаты показали, что наилучшие результаты достигаются при использовании более толстых стоматологических мембран.
Результаты серии исследований, касающихся толщины мембран, показывают, что мембраны большей толщины, расположены ли они в несколько слоев или один — проявляют большую барьерную функцию и дольше остаются в ткани, потому что медленно разлагаются и способствуют лучшей оссификации костного дефекта.
Хотя объяснить это открытие до сих пор не удалось, предполагается, что значительное увеличение толщины мембраны и долговечности приводит к увеличению ангиогенеза и клеточной популяции коллагенового матрикса, обуславливая пролиферацию, дифференцировку клеток и активную оссификацию.
Коллагеновые мембраны человеческого происхождения
Особое внимание следует уделить рассасывающейся коллагеновой мембране для стоматологии человеческого происхождения.
Роль рассасывающейся деминерализованной мембраны человека при направленной регенерации кости и направленной тканевой регенерации изучена недостаточно.
Ряд европейских исследований, посвященных изучению влияния толщины и происхождения резорбируемых мембран на регенерацию кости, дал противоречивые результаты.
Резорбируемая деминерализованная мембрана человека (RHDM) была получена из кости черепа трупа комбинацией физических и химических методов, а именно деминерализации кортикальной кости с последовательным удалением липопротеинов.
Эксперименты показали, что RHDM обеспечивает более высокую степень регенерации костной ткани по сравнению с другими мембранами, особенно при использовании более толстых мембран.
Комбинирование ростовых факторов
и мембран для стоматологии
В последнее время включение факторов роста и дифференциации в мембрану вызывают пристальный интерес исследователей.
Существует достаточно доказательств того, что определенные факторы роста и аналогичные медиаторы могут влиять на регенерацию многих тканей, в том числе на регенерацию костей.
Примером является разработка комбинированных мембран, которые могут контролировать высвобождение трансформирующего фактора роста (TGF-β).
Местная доставка широкого спектра факторов роста, таких как тромбоцитарные факторы роста (PDGF) и костные морфогенетические белки, которые являются остеоиндуктивными факторами роста, уже с успехом использовалась в стоматологии.
Эти вещества обладают способностью дополнительно стимулировать миграцию, пролиферацию и дифференцировку клеток. Многочисленные исследования in vitro, на животных и людях продемонстрировали преимущества перечисленных факторов в комбинации с коллагеновыми мембранами.
Такие инновации могут привести к серьезным изменениям в результатах направленной регенерации костной ткани без существенных дополнительных затрат.
Заключение
В этой статье рассматриваются основные принципы использования стоматологических мембран в направленной регенерации кости.
Значительный прогресс был достигнут с тех пор, как была использована оригинальная нерезорбируемая мембрана из политетрафторэтилена (e-PTFE).
Синтетические и природные биоматериалы применяют в стоматологической практике с большим клиническим успехом уже более 20 лет; их механические свойства и скорость биодеградации постоянно совершенствуются.
Ожидается, что следующее поколение мембран будет содержать новые функциональные молекулы, улучшающие результаты направленной регенерации кости.
Основные характеристики
Материал Cytoplast Regentex GBR 200 представляет собой плотную полимерную пленку толщиной 0,2 мм с гладкой поверхностью.
Последняя особенность является значительным преимуществом в сравнении с традиционными резорбируемыми мембранами, поверхность которых способствует ретенции и инвазии бактериями, вызывающими отторжение покрывного материала и воспаление раны.
Гладкая поверхность GBR-200 «отталкивает» патогенные микроорганизмы, не допуская инфицирования и воспаления операционной зоны.
Мембрана Cytoplast Regentex обладает микропористой структурой с размером пор до 1,26 мкр, которые не пропускают через пленку бактерий, но в то же время являются проницаемыми для протеинов.
Пластично-эластичная консистенция материала позволяет растягивать и деформировать его, предавая нужную форму для адаптации к операционной зоне.
Цитопласт обладает самоприклеивающим свойством к раневой поверхности. В качестве дополнительной меры фиксации может применяться ушивание краев лоскута, уложенного поверх Cytoplast, легкими без натяжения швами, не затрагивающими самой мембраны.
Материал поставляется со стандартными размерами 12х24 мм и 25х30 мм. Из этих заготовок можно вырезать ножницами куски любых размеров, необходимых в конкретной клинической ситуации.
Состав и свойства
Мембрана GBR-200 состоит из одного PTFE (политетрафторэтилена (тефлона)) – фтористоуглеродного соединения, устойчивого к воздействию практически любых агрессивных химических агентов.
В условиях человеческого тела PTFE абсолютно не растворяется веществами и физиологическими жидкостями.
Физико-химические и биологические свойства:
- химическая стабильность;
- предельно низкая аллергенность;
- самоприклеиваемость к ране;
- газо- и светонепроницаемость;
- непроницаемость для бактерий;
- проницаемость для протеинов.
Преимущества и недостатки
Cytoplast обладает целым рядом клинических и технологических преимуществ в сравнении с традиционными шовными материалами, благодаря чему пользуется большой популярностью у хирургов-стоматологов.
Преимущественные характеристики
- Отсутствие необходимости первичного лоскутного закрытия раневого фрагмента (не нужно готовить и натягивать лоскутный материал).
- Непрорастание эпителия, благодаря высоким барьерным свойствам материала.
- Эластичность (мембрана растягивается в любом направлении, адаптируясь к ране).
- Стабильность структуры (не набухает).
- Отсутствие необходимости закрывать мембрану чем-либо сверху, пленка может оставаться полностью обнаженной. Для полного закрытия раневого участка достаточно одного Cytoplast GBR-200.
- Самоприклеиваемость к ране, благодаря особой микроструктуре. Не требуется применения сложных фиксирующих элементов для крепления пленки к кости, края раны можно не ушивать.
- Отсутствие каких-либо негативных последствий и химических реакций при контакте материала с внутриротовой жидкостью.
- Быстрое заживление раны.
- Сохранение формы наращиваемой костной ткани альвеолярного отростка.
- Легкое безоперационное извлечение мембраны из раны через 21-25 дней. Удаление производится через небольшое отверстие с помощью зонда.
- Полное отсутствие каких-либо осложнений.
Недостатки
Многочисленные испытания не выявили ни одного существенного недостатка, которые нередко наблюдаются при использовании мембран другого типа.
Не было отмечено отторжения, воспаления, пролиферации и иных тканевых реакций, негативно сказывающихся на процессе заживления.
К единственному недостатку можно отнести необходимость для хирурга-стоматолога иметь практический навык использования материала, для чего приходится пройти предварительное обучение.
Показания
Мембрана GBR-200 рекомендуется к применению в стоматологии во всех случаях, связанных с направленной регенерацией кости:
- После удаления зубов для восстановления костной ткани альвеолярного отростка.
- Перед установкой имплантата при малом объеме кости.
- Во время или после установки имплантата – для закрытия раны.
- При аугментации в самых различных клинических случаях.
- При периимплантите (воспалении прилежащих к имплантату костных и мягких тканей, их резорбции и потере имплантата).
- При лоскутных операциях в ротовой полости, пластике и рецессии десны.
- При восстановлении челюстных пропорций (например, при плоскостной остеотомии, сопровождающейся подсадкой костной ткани между разъединенными фрагментами челюстных костей).
- При синус-лифтинге (Цитопласт укладывается на дно гайморовой пазухи для исключения риска проникновения остеозаменителя в синус через перфорации в слизистой оболочке).
Обсудим вместе плюсы и минусы имплантации зубов в сравнении с другими методиками протезирования.
В этой публикации мы расскажем, нужно ли пить антибиотики после имплантации зуба и зачем.
Пройдите по ссылке https://www.vash-dentist.ru/implantatsiya/metodiki/rashozhdeniya-shvov-posle-zubov.html, чтобы выяснить, когда снимают швы после имплантации зубов.
Что такое барьерные мембраны?
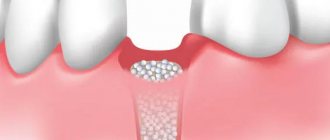
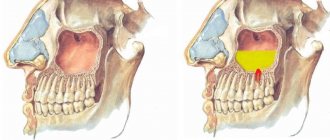
Барьерная мембрана — одно из самых современных и успешных изобретений в стоматологической практике. Такие конструкции активно используются практически во всех оперативных вмешательствах. Барьерные мембраны для костной пластики при имплантации позволяют предотвратить атрофические явления в альвеолярном отростке и способствуют одномоментной успешной фиксации искусственных корней. Мембрана влияет на регенераторные способности кости, увеличивая их, не пропускает внутрь опасные для костных клеток остеокласты и минимизирует риск проникновения патогенных агентов. Благодаря барьерной мембране приживление трансплантата ускоряется, как и общее лечение пациента.
Мембрана для костной пластики представляет собой очень тонкую и достаточно эластичную пластинку, которая крепится к кости титановыми штифтами. Таким образом происходит отделение десны от костного материала в процессе формирования натуральной ткани челюсти.
Виды мембран
Существует два типа барьерных мембран, которые широко используются в стоматологии:
- Резорбируемые. Такая конструкция постепенно рассасывается. Она не требует отдельного удаления, то есть дополнительного оперативного вмешательства, а значит приносит меньший травматизм.
- Нерезорбируемые. Мембраны такого типа самостоятельно не рассасываются, из-за чего пациенты нуждаются в дополнительном этапе лечения — удалении конструкции. В большинстве случаев они изготавливаются из титана. Крепятся такие мембраны при наличии серьезного дефицита костной ткани, восполненного гранулами остеогенного материала. После того, как альвеолярный отросток и мягкие ткани десны восстановятся, барьерная мембрана удаляется.
Стоматолог самостоятельно подбирает оптимальную мембрану для конкретного клинического случая. Он должен учитывать, что резорбируемые конструкции недостаточно хорошо фиксируют трансплантаты, поэтому их используют лишь при незначительных атрофиях.
Техника использования
После заполнения операционной раны костным заменителем поверх него укладывается Cytoplast GBR-200 с перекрытием на 2-3 мм краев раны. Помимо самоприклеивания пленка может фиксироваться на ране с помощью легкого без натяжения ушивания лоскутов, уложенных поверх Цитопласта.
Удаляется мембрана на 21-25 день с момента проведения операции. Предельный срок – 28 дней. Повторная операция для удаления Цитопласта не требуется.
Если поверх мембраны был уложен и ушит лоскут, извлечение (вытаскивание) материала производится с помощью зонда через небольшое отверстие. В большинстве случаев обезболивания при этом не требуется (в крайнем случае, используется аппликационная анестезия), кровотечения, как правило, не возникает.
После покрытия операционной раны под Цитопластом начинает быстро формироваться кость и вторичный эпителий. Сращивание лоскута с вновь образованным эпителием происходит обычно через месяц-полтора после операции.
В видео смотрите технику использования мембраны Цитопласт.
Диагностика
Для выявления эпиретинального фиброза необходимо исследование глазного дна, для чего назначается офтальмоскопия. Обследование в проходящем свете обнаруживает ее поблескивание над областью желтого пятна, напоминающее отражение от целлофановой пленки.
Эпиретинальная мембрана в начальной стадии очень тонкая, ее можно и не заметить, что затрудняет диагностику. Однако, если существует подозрение на ее наличие, для подтверждения диагноза, назначают ультразвуковое обследование. Также оно необходимо при непрозрачности оптических сред (стекловидного тела, хрусталика, роговицы), что затрудняет исследование глазного дна с помощью офтальмоскопии.
Еще одним диагностическим методом при эпиретинальном фиброзе является оптическая когерентная томография, которая помогает выяснить размер и структуру мембраны.
Степень нанесенного мембраной вреда дает возможность определить флюоресцентная ангиография, которая показывает масштаб макулярного отека. Насколько ухудшилось зрение пациента, определяют с помощью теста «решетка Амслера» и визометрии.
Рис.2 Витреоретинальный хирург в операционной при выполнении витрэктомиии и макулярного пилинга.
Клинические результаты
С целью определения эффективности мембраны GBR-200 разработчиком проводились исследования материала на группе из 10 пациентов в 3-х клинических случаях:
- экстирпация зуба;
- экстирпация зуба с подсадкой остеозаменителя;
- экстирпация зуба с имплантацией.
Обеспечивались следующие условия проведения операции:
- выкраивание мембраны выполнялось ножницами по форме дефекта;
- при наложении мембрана перекрывала лунку на 2-3 мм;
- прилегание материала к ране обеспечивалось растягиванием и прижатием пальцами и инструментом с учетом конфигурации альвеолярного отростка;
- Цитопласт оставался на ране 21 день, после чего осторожно стягивался пинцетом.
Результаты исследований
- Ни в одном случае применения материала GBR-200 не возникло воспалительного процесса, клеточной пролиферации или иных отрицательных тканевых реакций.
- Ни одна из мембран не была отторгнута.
- Все пленки были легко удалены с раны через 21 день без использования анестезии.
- На раневой поверхности, находившейся под мембраной, не отмечалось резорбции окружающих тканей и прорастания эпителия. Лишь в некоторых местах по краям раны имели место мигрирующие незначительные участки эпителия.
- Раневая поверхность после снятия Цитопласта представляла собой вновь образованную костную структуру.
По результатам исследования был сделан вывод, что при использовании Цитопласт GBR-200 в течение 3-х недель на поверхности раны был создан надежный барьер, предотвративший прорастание эпителиальной ткани.
Отзывы
Использование барьерных мембран при оперативных вмешательствах является новой, современной технологией, не получившей пока еще того распространения, которого она заслуживает.
Если вы подвергались операции с использованием барьерных мембран Цитопласт, поделитесь своим впечатления об этом материале с другими посетителями нашего сайта, оставьте свой комментарий внизу страницы.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Теги имплантация методы имплантации
Понравилась статья? Следите за обновлениями
Предыдущая статья
Спасать или удалять зуб при гнойном периодонтите?
Следующая статья
Универсальный трейнер I-3 для коррекции дефектов прикуса у детей
Виды резорбируемых мембран
Резорбируемыми называют рассасывающиеся мембраны, для производства которых используют следующие материалы.
- Полимеры, способные сохранять свои свойства на протяжении нескольких месяцев. К их достоинствам относят низкий риск развития аллергии и воспалительного процесса.
- Материал животного происхождения, характеризующийся высокой биосовместимостью с тканями челюсти человека. Такие мембраны используют реже, так как они могут спровоцировать аллергию.
Перед установкой барьерных мембран пациент проходит тщательное обследование для исключения риска развития осложнений.